Список литературы
1. Кравченко Н.А., Гаврилов Т.А., Хакимов М.И, Казанова В.Б., Васильева Е.И., Ботвинкин А.Д. Опыт сравнительного анализа заболеваемости пневмониями и острыми респираторными инфекциями верхних дыхательных путей после внедрения системы эпидемиологического мониторинга пневмоний.// Эпидемиология и Вакцинопрофилактика.- 2019. – Т.18. – №1. – С. 96-104.doi:10.31631/2073-3046-2019-18-1-96-104
2. Гапархоева З.М., Башкина О.А., Селиверстова Е.Н.Сравнительная характеристика триггерных механизмов формирования бронхообструктивного синдрома у детей с бронхиальной астмой и рецидивирующим обструктивным бронхитом. //Казанский медицинский журнал. – 2016. – Т. 97. – №1. – С. 66-69.doi:10.17750/KMJ2016-66
3. Бабаченко И.В., Самодова О.В., Анохин В.А., Михайлова Е.В. ,Богданова А.В.,Евдокимов К.В. . Клинико-эпидемиологические особенности респираторно-синцитиальной вирусной инфекции у детей первого года жизни. //Журнал инфектологии. – 2018. – Т. 10. -№3. – С. 70-76.doi.10.22625/2072-6732-2018-10-3-70-76
4. Смирнова А.О. Методы идентификации Streptococcus pneumoniae и характеристика его серотиповой принадлежности. // Успехи в химии и химической технологии. – 2017. – Т. 31. – №. 9. – C. 8-10.
5. Лазарева М.А., Куличенко Т.В., Алябьева Н.М., Пономаренко О.А., Лазарева А.В., Катосова Л.К.. Носоглоточное носительство Streptococcus pneumoniae у воспитанников детских домов, дошкольных учреждений и неорганизованных детей младше 5 лет. // Вопросы современной педиатрии. – 2015. – Т. 14. – №. 2. – С. 246-255.doi: 10.15690/vsp.v14i2.1293
6. Муравьев А.А., Козлов Р.С., Лебедева Н.Н. Эпидемиология серотипов S. pneumoniae на территории Российской Федерации. // Клиническая микробиология и антимикробная химиотерапия. – 2017. -Т. 19. № 3. – С. 200-206.
7. Tong S., Amand C., Kieffer A., Kyaw M.H. Trends in healthcare utilization and costs associated with acute otitis media in the United States during 2008-2014. // BMC Health Serv Res. -2018. –Vol. 18. – № 1. –P. 318. doi: 10.1186/s12913-018-3139-1.
8. Федосеенко М.В., Карнеева О.В., Галицкая М.Г., Поляков Д.П., Гайворонская А.Г. Острый средний отит у детей. Современный взгляд на проблему. Возможности вакцинопрофилактики. // Педиатрическая фармакология. – 2008. – Т. 5, № 4. -С. 25-29.
9. Grant L.R., Hammitt L.L., O’Brien S.E., Jacobs M.R., Donaldson C., Weatherholtz R.C. et al. Impact of the 13-valent pneumococcal conjugate vaccine on pneumococcal carriage among American Indians. // Pediatr. Infect. Dis. J. – 2016. – Vol. 35. – № 8. – P. 907–914. doi: 10.1097/INF.0000000000001207
10. Jallow S., Madhi S.A., Madimabe R., Sipambo N., Violari A., Kala U. Immunogenicity of 13-valent pneumococcal conjugate vaccine among children with underlying medical conditions. //Vaccine.-2017. – Vol. 35. – № 34. –P. 4321-4329. doi: 10.1016/j.vaccine.2017.06.081.
11. Зубова Е.С., Семериков В.В., Софронова Л. В., Костинов М.П. Оценка безопасности, иммуногенности и профилактической эффективности применения вакцины Превенар-13 у детей с бронхолегочной дисплазией. // Эпидемиология и вакцинопрофилактика. – 2018. – Т. 17. – № 2 (99). – С.65-69. doi:10.24411/2073-3046-2018-10009
12. Харит С.М., Фридман И.В., Павлюкова А.Н., Фролова Е.Я., Рулёва А.А. Клиническая эффективность пневмококковой конъюгированной 13-валентной вакцины у детей раннего возраста. // Педиатрическая фармакология. – 2016. – Т. 13, № 5. – С. 443-447.
13. Miller E., Andrews N.J., Waight P.A., Slack M.P., George R.C. Effectiveness of the new serotypes in the 13-valentpneumococcalconjugate vaccine. // Vaccine. – 2011. – Т. 29, № 49. –P. 9127-31. doi: 10.1016/j.vaccine.2011.09.112.
14. Zhou X., de Luise C., Gaffney M., Burt C.W., Scott D.A., Gatto N., et al. National impact of 13-valentpneumococcalconjugate vaccine on ambulatory care visits forotitismedia in children under 5 years in the United States. //Int J Pediatr Otorhinolaryngol. – 2019. – Vol. 119. – P. 96-102. doi: 10.1016/j.ijporl.2019.01.023.
Побочные действия
Безопасность вакцины Превенар 13 изучена у здоровых детей (4429 детей/14267 доз вакцины) от 6 недель до 11–16 мес и 100 детей, родившихся недоношенными (в срок <37 недель гестации). Во всех исследованиях вакцина Превенар 13 применялась одновременно с другими вакцинами, рекомендованными для данного возраста.
Кроме того, безопасность вакцины Превенар 13 оценена у 354 детей в возрасте 7 мес — 5 лет, ранее не вакцинированных ни одной из пневмококковых конъюгированных вакцин. Наиболее частыми нежелательными реакциями были реакции в месте инъекции, повышение температуры, раздражительность, снижение аппетита и нарушение режима сна. У детей старшего возраста при первичной вакцинации вакциной Превенар 13 наблюдалась более высокая частота местных реакций, чем у детей первого года жизни.
При вакцинации вакциной Превенар 13 недоношенных детей (родившихся при сроке гестации ≤37 недель), включая глубоко недоношенных детей, родившихся при сроке беременности менее 28 нед, и детей с экстремально низкой массой тела (≤500 г) характер, частота и выраженность поствакцинальных реакций не отличались от таковых у доношенных детей.
У лиц 18 лет и старше отмечалось меньшее количество побочных эффектов, вне зависимости от предшествующих вакцинаций. Однако частота развития реакций была такая же, как и у привитых более молодого возраста.
В целом частота побочных эффектов была одинакова у пациентов возрастных групп 18–49 лет и у пациентов старше 50 лет, за исключением рвоты. Данный побочный эффект у пациентов 18–49 лет встречался чаще, чем в возрасте старше 50 лет.
У взрослых пациентов с ВИЧ-инфекцией отмечалась такая же частота побочных реакций, как и у пациентов 50 лет и старше, за исключением лихорадки и рвоты, которые наблюдались очень часто, и тошноты, которая наблюдалась часто.
У пациентов после трансплантации гемопоэтических стволовых клеток частота развития побочных реакций была такая же, как и у здоровых взрослых пациентов, за исключением лихорадки и рвоты, которые у этих пациентов встречались очень часто. У детей и подростков с серповидноклеточной анемией, ВИЧ-инфекцией или после трансплантации гемопоэтических стволовых клеток отмечалась такая же частота побочных реакций, как и у здоровых пациентов 2–17 лет, за исключением головной боли, рвоты, диареи, лихорадки, утомляемости, артралгии и миалгии, которые у таких пациентов встречались как очень частые.
Нежелательные реакции, перечисленные ниже, классифицированы в соответствии с частотой их проявления во всех возрастных группах следующим образом: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1000, но <1/100); редко (≥1/10000, но < 1/1000) и очень редко (<1/10000).
Нежелательные реакции, выявленные в клинических исследованиях вакцины Превенар 13
Очень часто — гипертермия; раздражительность; покраснение кожи, болезненные ощущения, уплотнение или отек размером 2,5–7,0 см в месте инъекции (после ревакцинации и/или у детей 2–5 лет); рвота (у пациентов 18–49 лет), сонливость, ухудшение сна, ухудшение аппетита, головная боль, генерализованные новые или обострение имеющихся болей в суставах и мышечных болей, озноб, утомляемость.
Часто — гипертермия выше 39 °C; болезненность в месте инъекции, приводящая к кратковременному ограничению объема движений конечности; гиперемия, уплотнение или отек размерами 2,5–7,0 см в месте введения вакцины (после серии первичной вакцинации у детей в возрасте до 6 мес), рвота, диарея, сыпь.
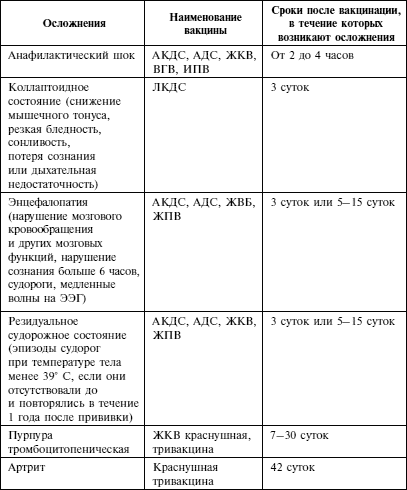
Нечасто — покраснение кожи, уплотнение или отек размерами более 7,0 см в месте инъекции; плаксивость, судороги (включая фебрильные судороги), реакции гиперчувствительности в месте инъекции (крапивница, дерматит, зуд)**, тошнота.
Редко — случаи гипотонического коллапса*, приливы крови к лицу**, реакция гиперчувствительности, включая одышку, бронхоспазм, отек Квинке разной локализации, включая отек лица**, анафилактическая/анафилактоидная реакция, включая шок**, лимфаденопатия в области места инъекции.
Очень редко — регионарная лимфаденопатия**, полиформная эритема**.
*Наблюдались только в клинических исследованиях вакцины Превенар, однако возможны и для вакцины Превенар 13.
**Отмечались при постмаркетинговых наблюдениях вакцины Превенар; их можно рассматривать как вполне возможные и для вакцины Превенар 13.
Нежелательные явления, наблюдавшиеся в других возрастных группах, также могут проявляться у детей и подростков 5–17 лет. Однако в клинических исследованиях их не отмечали из-за небольшого количества участников.
Значимых различий в частоте развития побочных эффектов у взрослых, ранее вакцинированных и невакцинированных ППВ23, не отмечено.
Наблюдение после вакцинации
Если говорить именно о риске гипертермии, то после прививки надо измерять температуру каждый 4-6 часов. Если температура заметно повышается, проверяйте чаще и начинайте её сбивать
Обращаем внимание, что гипертермия может вернуться даже после стабилизации температуры, поэтому проверяйте её в течение недели после вакцинации
Нет единого мнения по поводу того, надо ли сбивать температуру после прививки, но обычно руководствуются теми же принципами, что при обычном вирусном заболевании: до 38 градусов вмешиваться не стоит, а выше – давать жаропонижающие. Впрочем, это всё очень индивидуально, и бывают ситуации, когда надо реагировать даже на невысокую температуру, например, при заметном общем ухудшении состояния или при склонности к судорогам и неврологических болезнях.
Как облегчить состояние
Поствакцинальные реакции – это ведь не только повышенная температура, поэтому для начала создайте спокойную обстановку, не заставляйте детей постоянно лежать в кровати – они этого не любят, не нагружайте какими-нибудь делами, воздержитесь от прогулок. Из общих рекомендаций – регулярно проветривать комнату, давать больше жидкости и не заставлять есть насильно, так как после прививки аппетит снижается. Особо стоит отметить запрет на аспирин – у него слишком много побочных эффектов.
Что касается методов снижения температуры, то они такие же, как при любых вирусных болезнях: дать Парацетамол или Нурофен, обтирать влажной салфеткой – у каждого свои любимые способы, мы не будем здесь их описывать.
Особенности гипертермии у грудничков
Одна из особенность грудных детей – у них нормальная температура примерно 37.3 градуса, а её повышение после прививок наблюдается реже
Важно также знать, что гипертермия у грудничков развивается гораздо стремительнее, поэтому меры надо принимать уже при небольшом повышении температуры до 37.5 градусов
Так что же это за инфекция – пневмококковая?
Это комплекс заболеваний, вызываемых бактерией Streptococcus pneumoniae (пневмококк): пневмококковая пневмония (до 70 % от всех пневмоний), острый средний отит (около 25 % от всех отитов), гнойный пневмококковый менингит (5-15 % всех бактериальных менингитов), эндокардиты (около 3 %), плевриты, артриты. Пневмококковая инфекция, как правило, является осложнением других инфекций — примером этого являются пневмококковая пневмония после перенесённого гриппа или кори, воспаление среднего уха (отит) у детей после или на фоне любой респираторной вирусной инфекции.
Возбудитель пневмококковой пневмонии, Streptococcus pneumoniae, является представителем нормальной микрофлоры верхних дыхательных путей человека. В норме носителями одного или нескольких типов пневмококков являются от 5 до 70 % людей. У «организованных» (проживающих или находящихся в коллективах) детей и взрослых уровень носительства максимален. К настоящему времени выделено более 90 различных серотипов (иммунологических вариантов) пневмококков, все они потенциально патогенны, тяжелые инфекции вызывают примерно два десятка из них. Самая высокая заболеваемость тяжелыми пневмококковыми инфекциями регистрируется у детей в возрасте до 5 лет и среди пожилых людей (старше 65 лет). Именно в этих возрастных группах, грипп и пневмонии занимают первое место как причина смерти среди всех инфекций и 5-е место среди всех причин смерти.
Пневмококковая инфекция распространяется воздушно-капельным путём, например при кашле, особенно при тесном контакте. Источником инфекции может быть человек без всяких клинических проявлений. Чаще всего это случается зимой или ранней весной. Когда возбудитель попадает в лёгкие, он может вызвать пневмонию. Он также может проникать в кровеносное русло и вызывать бактериемию, попадая в ткани, окружающие головной или спинной мозг, вызывает гнойный менингит.
Инкубационный период пневмококковой инфекции длится от 1 до 3 дней.
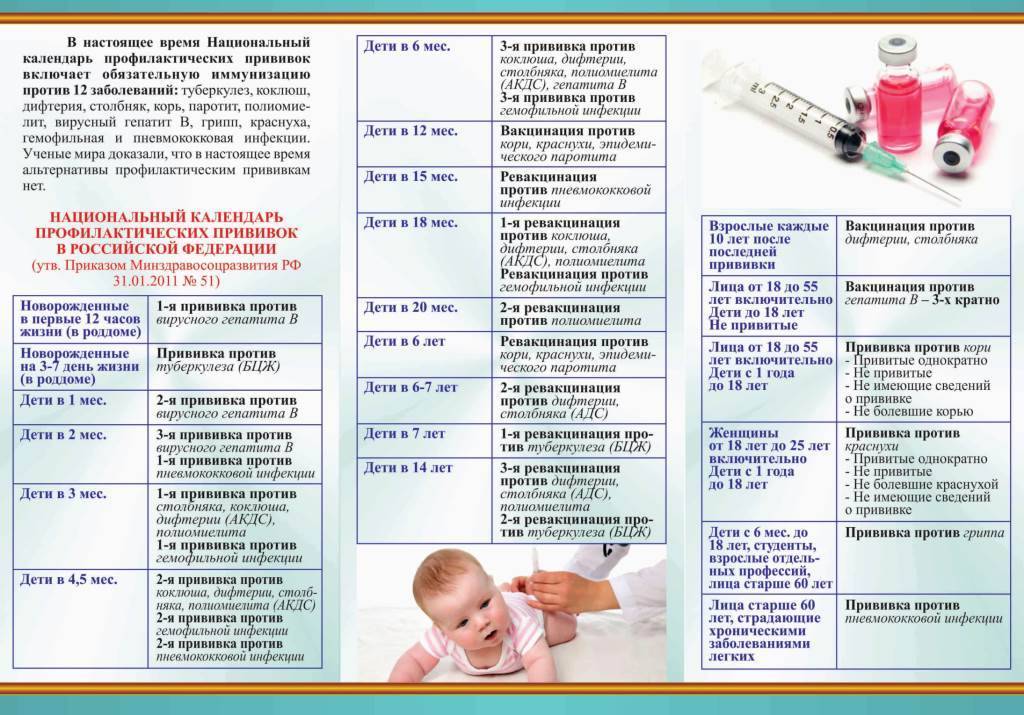
Определения серологических типов пневмококка в России в широкой практике не проводится, однако российское исследование показало, у больных выделяются как раз те серотипы, которые включены в состав 23-валентной пневмококковой вакцины. Вакцина содержит только части убитых микроорганизмов (очищенные капсульные полисахариды). Государственный реестр лекарственных средств России в категории «Вакцина для профилактики пневмококковых инфекций» содержит следующие препараты: Превенар, Превенар 13, Пневмо 23, Пневмовакс 23, Синфлорикс.
Доступность вакцинации для детей и лиц старшего возраста обеспечивается включением ее в Национальный календарь профилактических прививок ( Приказ МЗ РФ от 21 марта 2014 года №125н).
Состав
Суспензия для внутримышечного введения | 1 доза (0,5 мл) |
активные вещества: | |
пневмококковые конъюгаты (полисахарид — CRM197): | |
полисахарид серотипа 1 | 2,2 мкг |
полисахарид серотипа 3 | 2,2 мкг |
полисахарид серотипа 4 | 2,2 мкг |
полисахарид серотипа 5 | 2,2 мкг |
полисахарид серотипа 6A | 2,2 мкг |
полисахарид серотипа 6B | 4,4 мкг |
полисахарид серотипа 7F | 2,2 мкг |
полисахарид серотипа 9V | 2,2 мкг |
полисахарид серотипа 14 | 2,2 мкг |
олигосахарид серотипа 18С | 2,2 мкг |
полисахарид серотипа 19А | 2,2 мкг |
полисахарид серотипа 19F | 2,2 мкг |
полисахарид серотипа 23F | 2,2 мкг |
белок-носитель CRM197 | »32 мкг |
вспомогательные вещества: алюминия фосфат — 0,5 мг (в пересчете на алюминий — 0,125 мг); натрия хлорид — 4,25 мг; янтарная кислота — 0,295 мг; полисорбат 80 — 0,1 мг; вода для инъекций — до 0,5 мл |
Побочные эффекты
Как и любая другая прививка, эта, может, приводить к реакциям со стороны организма. Из, наиболее часто встречающихся, могут наблюдаться следующие побочные эффекты.
- Повышение температуры после прививки «Превенар».
- Приблизительно у трети привитых наблюдалась местная болезненная реакция на введение препарата и незначительная слабость в конечности.
- Возможны местные и общие аллергические реакции.
- Увеличение групп лимфатических узлов.
- После прививки ребёнок в течение непродолжительного времени может быть нервным, раздражительным, вялым, сонливым.
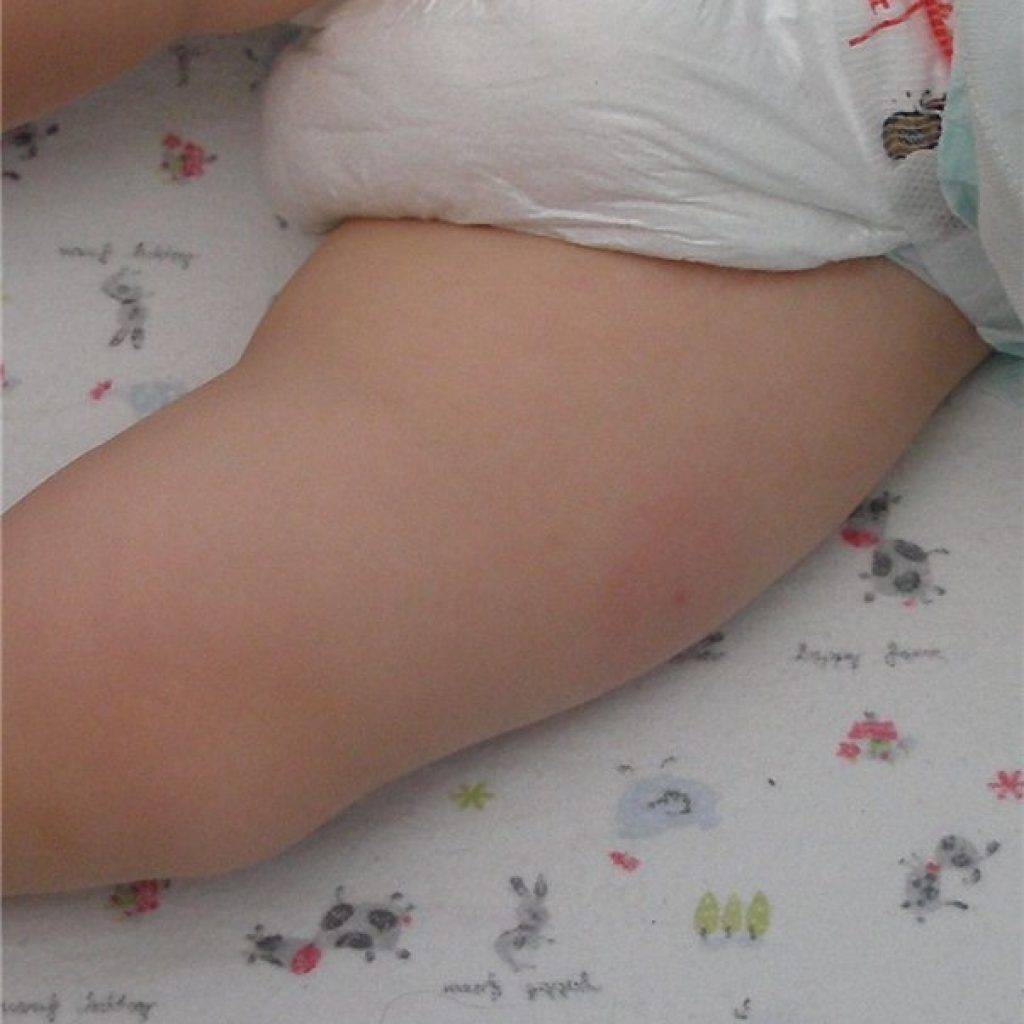
- После прививки «Превенар» наблюдаются покраснения и уплотнения в месте инъекции. Эти осложнения характерны для более старших детей.
- Нарушение аппетита, тошнота и рвота.
- Редко бывают судороги и апноэ (временная остановка дыхания, больше характерна для детей с недоразвитой дыхательной системой).
- Возможны и более тяжёлые реакции — анафилактический шок, бронхоспазм и отёк Квинке.
Согласно календарю прививок, препарат может вводиться одновременно с другими вакцинами (АКДС), поэтому точно определить на какой из них возникли осложнения иногда сложно
Важное условие после использования вакцины «Превенар» — в течение как минимум 30 минут оставаться под наблюдением медработников. Это необходимо, чтобы вовремя среагировать на возможные нежелательные реакции организма
В случае появления любых осложнений, которые не проходят в течение суток (за исключением шока, бронхоспазма, отёка Квинке, рвоты и других тяжёлых состояний) следует вызвать врача.